Verschil tussen hard water en zwaar water | Hard Water vs Heavy Water
Belangrijkste verschil - hard water tegen zwaar water
Het belangrijkste verschil tussen hard water en zwaar water is hun samenstelling, aangezien beide typen "hard water" en "zwaar water" naar het water verwijzen met twee waterstofatomen en een zuurstofatoom in het watermolecuul. Als we de moleculaire samenstelling van zwaar water overwegen, bevat het meer deuteriumatomen dan waterstofatomen. De moleculaire samenstelling van het hard water is hetzelfde als het normale water, maar de minerale samenstelling (Magnesium-Mg en Calcium-Ca) is relatief hoger dan de zacht water.
Wat is zwaar water?
Een watermolecuul bevat twee waterstofatomen en een zuurstofatoom. Waterstof heeft drie isotopen; protium (99,98%), deuterium en tritium. Protium heeft één elektron en een neutron. Deuterium heeft naast het elektron en het proton een neutron in de kern. Deuterium is tweemaal zwaarder dan het meest voorkomende waterstofatoom.
Zwaar water bevat een groot deel van deuteriumatomen dan het gebruikelijke waterstofatoom. Daarom is het molecuulgewicht en de dichtheid hoger dan het normale water. Men zegt dat de dichtheid van zwaar water 11 keer groter is dan dat van normaal water.
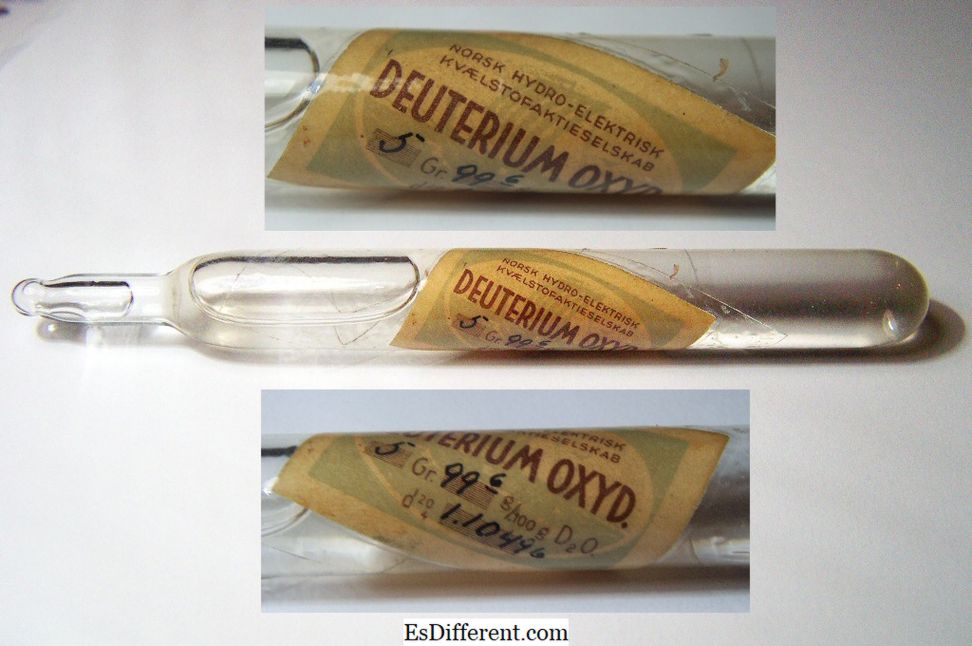
Een historische steekproef van "zwaar water", verpakt in een afgesloten capsule.
Wat is hard water?
In het algemeen bevat water een aantal mineralen, zoals magnesium, calcium en kalium. Maar hard water bevat meer mineralen, in het bijzonder Magnesium (Mg) en Calcium (Ca) dan normaal water (zacht water). Vanwege dit feit is de hardheid van het harde water groter dan de hardheid van het normale water. Dit gebeurt wanneer het oppervlaktewater door de grond in de grondwaterlaag stroomt door de mineralen in het vrijstromende water op te lossen.
Hard water zorgt niet voor schadelijke gevolgen voor de menselijke gezondheid, maar veroorzaakt zo veel extra problemen, zoals het verlaten van witte kleurstoffen in koken of kookinstallaties, badkamervloeren en waterleidingen.

Wat is het verschil tussen hard water en zwaar water?
Definitie van hard water en zwaar water
Zwaar water: Zwaar water is water met een aanzienlijk deel van deuteriumatomen, gebruikt in kernreactoren
Hard Water: Hard Water is water dat bevat een opmerkelijke hoeveelheid opgeloste zouten van calcium en magnesium.
Eigenschappen van hard water en zwaar water
Samenstelling
Zwaar water: Zwaar water bevat een groot deel van deuterium (bevat een extra neutron in de kern) atomen dan het normale water.Het bevat zowel waterstofatomen als deuteriumatomen die de watermoleculen vormen die de moleculaire formule hebben als D 2 O (Deuterium Oxide) en HDO (Hydrogen-Deuterium Oxide).
Hard Water: Op het moleculaire niveau is de samenstelling van hard water vergelijkbaar met die van normaal water (H 2 O). Maar, het bevat meer mineralen; Magnesium en Calcium dan het normale drinkwater.
Fysische en chemische eigenschappen
Zwaar water: Fysische en chemische eigenschappen van zwaar water zijn vergelijkbaar met het normale water, maar het heeft een hoge dichtheidswaarde. Het molecuulgewicht van het zware water laat geen significante verandering zien, omdat het enkele zuurstofatoom ongeveer 89% draagt bij het molecuulgewicht. Biologische eigenschappen van zwaar water verschillen van het normale water.
Hard Water: Hardheid is de belangrijkste eigenschap die significant verschilt van normaal water.
USGS classificatie van waterhardheid
- diff Artikel Midden voor tafel ->| Hardheid / mgl -1 | Aard van het water |
| 0-60 | Zacht water |
| 61- 120 | Matig hard water |
| 121- 180 | Hard water |
| <180 | Zeer hard water |
De aanbevolen hardheidsgraad in drinkwater is 80-100 mgl -1
Gezondheidseffect < Heavy Water:
Er is een hoeveelheid Deuterium aanwezig in het menselijk lichaam, maar een groot aantal Deuterium veroorzaakt schadelijke gevolgen voor de gezondheid in het menselijk lichaam, het kan zelfs de dood veroorzaken. Hard Water:
Hard water zorgt voor geen gezondheidseffecten in het menselijk lichaam, maar zorgt ervoor dat er andere problemen zijn, zoals het stoppen van waterpijpen en het verlaten van minerale afzettingen op verwarmers, kookapparatuur en badkamervloeren. Om deze problemen te voorkomen die door het harde water worden veroorzaakt, worden de mineralen verwijderd. Dit heet softening. De meest gebruikte effectieve methode is de ionenuitwisselingsharsen als verzachter. Image Courtesy:
"Druppelkraan 1" door Gebruiker: Dschwen - Eigen werk. (CC BY-SA 2. 5) via Wikimedia Commons "Deuteriumoxide Norsk" door Alchemist-hp (talk) (www. Pse-mendelejew. De) - Eigen werk. (FAL) via Commons




