Verschil tussen destillatie en extractie | Distillatie vs Extractie
Belangrijkste verschil - Distillatie versus Extractie
Hoewel destillatie en extractie twee van de meest gebruikte fysieke scheidingsmethoden zijn, die gelijke mate hebben in de industrie om zuivere chemicaliën te verkrijgen voor veel toepassingen bestaan er een verschil tussen destillatie en extractie op basis van hun procedures. Het sleutelverschil tussen destillatie en extractie is dat destillatie volgt op het verwarmen van een vloeibaar mengsel en de damp van de vloeistof bij hun kookpunt t verzamelt en de damp condenseren om de pure stof terwijl, bij extractie, een geschikt oplosmiddel wordt gebruikt voor het scheidingsproces.
Wat is distillatie?
Distillatie is een van de oudste, maar nog steeds meest gebruikte methode voor het scheiden van vloeibare mengsels, op basis van de verschillen in hun kookpunten. Het omvat het verwarmen van een vloeibaar mengsel geleidelijk om de kookpunten van de vloeistoffen in het mengsel te bereiken, hun damp op verschillende kookpunten te krijgen en wordt gevolgd door condensatie van de damp om de zuivere stof in vloeibare vorm te verkrijgen.
De vloeistoffen met lagere kookpunten (de meest vluchtige stoffen) worden eerst afgekookt als het mengsel wordt verwarmd, terwijl minder vluchtige stoffen in het mengsel blijven totdat de temperatuur in het mengsel tot hun kookpunt komt. Voor het destillatieproces wordt een speciaal ontwerpset apparaat gebruikt.

Wat is Extractie?
Het extractieproces houdt in het terugtrekken van een actief middel of een afvalstof uit een vast of vloeibaar mengsel onder gebruikmaking van een geschikt oplosmiddel. Het oplosmiddel is niet geheel of gedeeltelijk mengbaar met de vaste stof of de vloeistof, maar is mengbaar met het actieve middel. Het actieve middel overbrengt van het vaste of vloeibare mengsel naar het oplosmiddel door intensief contact met de vaste stof of de vloeistof. De gemengde fasen in het oplosmiddel worden gescheiden door centrifugeren of zwaartekracht scheidingswerkwijzen.

Extractie van Petroleum
Wat is het verschil tussen Distillatie en Extractie?
Distillatie- en extractiemethoden
Distillatiemethode
Beschouw een vloeibaar mengsel met vier vloeistoffen, A, B, C en D.
Kookpunten: Bp vloeibaar A (T T Bp vloeibaar B (T B ) > Bp vloeibaar C (T C ) > Bp vloeibaar D (T D ) (Minst vluchtige verbinding) (Mest vluchtige verbinding) Temperatuur van het mengsel = T m Bij het verwarmen van het vloeibare mengsel verlaat de meest vluchtige vloeistof (D) het mengsel eerst wanneer de temperatuur van het mengsel gelijk is aan het kookpunt (T
m = T

D) terwijl andere vloeistoffen in het mengsel blijven.De damp van vloeistof D wordt verzameld en gecondenseerd om zuivere vloeistof D te krijgen. Als de vloeistof verder wordt verhit, koken de andere vloeistoffen ook op hun kookpunten af. Naarmate het destillatieproces doorloopt, neemt de temperatuur van het mengsel toe. Extractiewerkwijze Beschouw een actieve stof A is in vloeibare B en ze zijn volledig mengbaar. Het oplosmiddel C wordt gebruikt om A van B. Vloeistof B te scheiden en vloeistof C zijn niet mengbaar. 1: Stof A wordt opgelost in vloeistof A 2: Na het toevoegen van oplosmiddel C gaan sommige van de moleculen in vloeistof A naar oplosmiddel C
3: Naarmate de tijd verloopt, gaan meer moleculen naar het oplosmiddel C.
(Oplosbaarheid van A in het oplosmiddel is groter dan die van vloeistof A)
4: Oplosmiddel C wordt gescheiden van vloeistof A aangezien deze niet mengbaar zijn. Een andere methode wordt gebruikt om A van het oplosmiddel te isoleren.
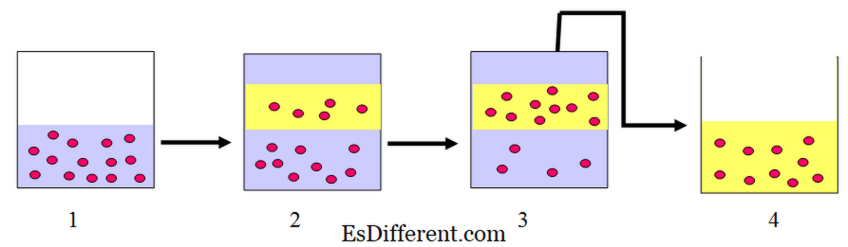
Meerdere extracties worden gedaan om volledig A te scheiden van oplosmiddel B. Temperatuur is constant in dit proces.
Distillatie- en extractietypes
Distillatie: De meest gebruikte destillatiemethoden zijn "eenvoudige destillatie" en "fractionele destillatie. "
Eenvoudige destillatie
wordt gebruikt wanneer de vloeistoffen die gescheiden zijn, nogal verschillende kookpunten hebben.
Fractionele destillatie
wordt gebruikt wanneer de twee vloeistoffen die worden gescheiden, bijna dezelfde kookpunten bezitten. Extractie: De meest voorkomende extractie types zijn "vaste-vloeistof extractie" en "vloeistof-vloeistof extractie. " Vloeibare extractie houdt in dat een stof wordt gescheiden van een vaste stof met behulp van een oplosmiddel. Vloeistof - vloeibare extractie
omvat het isoleren van een stof uit een vloeistof met behulp van een oplosmiddel. Toepassingen van destillatie en extractie Distillatie: Deze scheidingsmethode wordt gebruikt bij de fractionele destillatie van ruwe olieproductie, chemische en aardolieindustrie. Bijvoorbeeld, benzeen uit tolueen, ethanol of methanol uit water en azijnzuur uit aceton scheiden. Extractie: Het wordt gebruikt om organische verbindingen zoals fenol, aniline en nitraat aromatische verbindingen uit water te isoleren. Het is ook handig om essentiële oliën, farmaceutica, smaken, geuren en voedingsmiddelen te verwijderen.




