Verschil tussen atoom- orbitaal- en hybride orbitaal
Atomic Orbital vs Hybrid Orbital
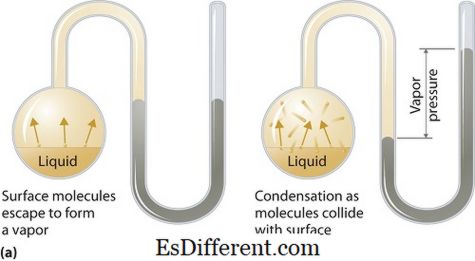
De binding in moleculen werd op een nieuwe manier begrepen met de nieuwe theorieën die Schrodinger, Heisenberg, en Paul Diarc presenteren. De kwantummechanica kwam in de foto met hun bevindingen. Zij vonden dat een elektron zowel deeltjes- als golfeigenschappen heeft. Hiermee ontwikkelde Schrodinger vergelijkingen om de golfaard van een elektron te vinden en kwam de golfvergelijking en de golffunctie op. Golffunctie (Ψ) komt overeen met verschillende toestanden voor het elektron.
Atomic orbital
Max Born wijst op een fysieke betekenis aan het vierkant van de golffunctie (Ψ 2 ) nadat Schrodinger zijn theorie heeft voorgesteld. Volgens Born, expresseert Ψ 2 de kans op het vinden van een elektron op een bepaalde locatie. Dus, als Ψ 2 een grotere waarde is, dan is de kans op het vinden van het elektron in die ruimte hoger. Daarom is in de ruimte de waarschijnlijkheidsdichtheid van de elektronen groot. In tegendeel, als Ψ 2 laag is, dan is de electronwaarschijnlijkheidsdichtheid daar laag. De plots van Ψ 2 in x, y en z axes tonen deze waarschijnlijkheden en hebben de vorm van s, p, d en f orbitals. Deze staan bekend als atoom-orbitalen. Een atoomwand kan gedefinieerd worden als een gebied van ruimte waar de kans op het vinden van een elektron groot is in een atoom. Atoom-orbitalen worden gekenmerkt door kwantumgetallen, en elke atoombaan kan twee elektronen tegengaan met tegenovergestelde spins. Als we bijvoorbeeld de elektronconfiguratie schrijven, schrijven we als 1s 2 , 2s 2 , 2p 6 , 3s 2 . 1, 2, 3 …. n integerwaarden zijn de kwantumgetallen. Het superscript nummer na de orbitale naam toont het aantal elektronen in die orbitaal. s orbitals zijn bolvormig en klein. P-orbitalen zijn dumbbellvormig met twee lobben. Een lap wordt gezegd positief, en de andere lob is negatief. De plaats waar twee lobben elkaar aanraken is bekend als een knooppunt. Er zijn 3 p orbitalen als x, y en z. Ze zijn in de ruimte geregeld, zodat hun assen loodrecht op elkaar liggen. Er zijn vijf d orbitals en 7 f orbitals met verschillende vormen. Zo gezamenlijk, hierna volgt het totale aantal elektronen dat in een orbitaal kan verblijven.
s orbitale-2 elektronen
P orbitals-6 elektronen
d orbitals-10 elektronen
f orbitals- 14 elektronen
Hybride orbitaal
Hybridisatie is het mengen van twee niet-equivalent atoomorganen. Het resultaat van hybridisatie is de hybride orbitale. Er zijn vele soorten hybride orbitalen gevormd door s, p en d orbitals te mengen. De meest voorkomende hybride orbitalen zijn sp 3 , sp 2 en sp. Bijvoorbeeld, in CH 4 heeft C 6 elektronen met de elektronconfiguratie 1s 2 2s 2 2p 2 bij de grondtoestand.Wanneer opgewonden, beweegt één elektron op het niveau van 2s naar het 2p-niveau en geeft drie 3 elektronen. Dan mengen de 2s elektronen en de drie 2p elektronen elkaar en vormen vier equivalente sp 3 hybride orbitalen. Evenzo worden bij hybridisatie drie hybridhybride orbitalen en sp- 2 twee hybridische orbitalen gevormd. Het aantal geproduceerde hybride orbitalen is gelijk aan de som van orbitalen die gehybridiseerd worden.